어느 메타과학자들의 고백과, 오픈액세스가 교리이기를 멈춰야 하는 이유
초파리 유전학자의 냉동고에는 내가 만들지 않은 생명들이 잠들어 있다. 수십 년 전 누군가가 처음 분리해낸 돌연변이 계통, 한 번도 그 정체를 의심해본 적 없는 균형 염색체, 작은 라벨 하나로만 신원을 증명하는 수백 개의 바이알. 나는 그 병 속의 파리가 라벨에 적힌 바로 그 유전형이라고 믿는다. 직접 확인한 적은 없다. 사실 확인할 방법도 마땅치 않다. 내 실험의 아홉 할은 이렇게, 얼굴도 모르는 동료들이 남긴 신원의 정직함 위에 얹혀 있다. 뉴턴이 말한 거인의 어깨란 천재의 우람한 등이 아니라, 누가 언제 채워 넣었는지조차 모를 이 거대한 재고 더미였는지도 모른다. 그 재고를 믿을 수 있다는 단 하나의 전제 위에서만, 나는 오늘 아침에도 새 실험을 시작한다.
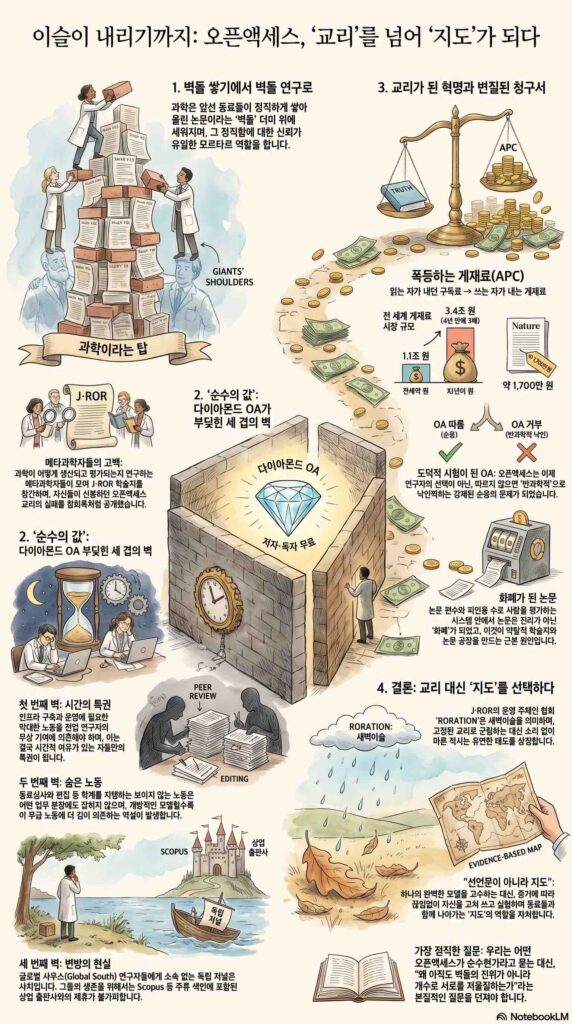
그런데 요즘 나는 그 전제를 정면으로 흔드는 고백문을 읽는다. 재고를 채워 넣는 사람의 고백이 아니라, 재고의 출처를 감사(監査)하는 사람들의 고백이다. 올해 5월, 테일러 앤 프랜시스(Taylor & Francis)에서 『연구에 관한 연구 저널(Journal of Research on Research, 이하 J·ROR)』이라는 낯선 학술지가 창간됐다. 그 창간사는 한 편의 학술 선언이라기보다 차라리 참회록에 가깝다. 편집자들은 자신들이 그토록 오래 설교해온 오픈액세스(OA)의 이상을 스스로 지키지 못했음을, 그 실패의 전 과정을 공개한다. 그들은 그것을 “선언문이 아니라 지도”라고 불렀다. 나는 이 문장 하나에 오픈액세스 운동 사반세기의 결론이 담겨 있다고 생각한다.
이 글은 그 고백문을 천천히 따라 읽으면서, 한 가지 불편한 결론에 이르려 한다. 오픈액세스는 더 이상 교조적인 이념이어서는 안 된다는 것. 그리고 그 사실을 가장 정직하게 증명한 사람들이, 다름 아닌 우리를 연구하는 메타과학자들이었다는 것.
거인의 어깨를 연구하는 사람들
먼저 이들이 누구인지부터 말해야겠다. ‘연구에 관한 연구(research-on-research)’는 과학계량학, 과학기술학(STS), 과학사회학, 연구평가학, 메타리서치를 한데 묶는, 비교적 최근에 별자리처럼 모여든 분야다. 쉽게 말해 과학이 어떻게 생산되고 평가되고 통치되는지를 과학적으로 연구하는 사람들이다. 약탈적 학술지가 무엇인지, 영향력지수가 어떻게 과학을 왜곡하는지, APC(논문 게재료)가 어떻게 불평등을 심화하는지를 논문으로 써내는 바로 그 집단이다.
J·ROR을 만든 제마 데릭, 바트 펜더스, 토니 로스-헬라우어, 세르게 호르바흐는 이 분야의 핵심 인물들이다. 그리고 이들의 이야기는 깊은 아이러니에서 출발한다. 이들은 본래 MDPI라는 출판사가 내는 『퍼블리케이션스(Publications)』라는 저널의 편집진이었다. 출판 윤리와 약탈적 출판을 다루는 논문을 심사하고 게재하던 저널이다. 그런데 정작 그 모회사 MDPI는, 2021년 옥스퍼드대 출판부의 『리서치 이밸류에이션』에 실린 한 분석에서 비정상적으로 높은 자기인용률을 지적당하며 약탈적 출판의 혐의를 받았고, 일부 저널은 클래리베이트의 웹 오브 사이언스에서 색인 취소를 당했으며, 핀란드의 출판포럼에서는 ‘레벨 0’ 등급으로 강등됐다.
약탈적 출판을 비판하는 논문을 펴내는 편집자가, 약탈적이라 손가락질받는 출판사의 우산 아래 앉아 있었던 것이다. 그들 자신의 표현을 빌리면, 그들은 자기 비판으로부터 면제되지 않았다. 오히려 더 큰 책임을 져야 했다. 편집위원 다수가 불안정한 초기 경력 연구자였고, 그들은 자기 나라의 평가 목록 때문에 정작 자기 저널에는 자기 논문을 싣기를 꺼렸다. 그 모순이 임계점을 넘은 2023년, MDPI 측이 한번 거절된 원고를 재고해달라고 요청해 편집 독립성을 위협하자, 데릭과 펜더스는 사임했고 편집위원 대다수가 뒤따랐다. 흥미롭게도 이들의 재임 기간 동안 『퍼블리케이션스』는 단 한 푼의 게재료도 받지 않았다. 그러나 그들이 떠난 직후 MDPI는 그 저널에 1600 스위스프랑의 게재료를 매겼다. 게재료가 없던 시절 그 저널의 가치는 수익이 아니라, 다른 유료 저널들이 약탈적이라는 비난을 받을 때 내세울 수 있는 ‘점잖음의 방패’였던 셈이다.
여기까지가 J·ROR의 전사(前史)다. 그리고 진짜 이야기는 그들이 떠난 다음에 시작된다. 이상적인 저널을 처음부터 새로 만들면 되지 않겠는가. 게재료 없는, 완전히 공개된, 공동체가 소유하는 저널. 다이아몬드 오픈액세스. 그것이 이 분야가 신봉하는 교리였다.
순수의 값
다이아몬드 오픈액세스는 아름다운 이상이다. 저자도 독자도 한 푼 내지 않고, 공동체가 직접 소유하고 운영하는 저널. 유네스코도, 유럽위원회도 이 모델을 밀고 있다. 그러니 OA를 평생 설파해온 이 메타과학자들이 자기 저널만큼은 다이아몬드로 만들려 한 것은 당연했다. 그런데 막상 만들려 하자 이상이 현실의 벽에 부딪혔다. 창간사가 고백하는 그 벽은 세 겹이었다.
첫째는 시간이라는 이름의 특권이다. 저널 하나를 맨바닥에서 세우려면 투고 시스템, 동료심사 인프라, 디지털 호스팅, 홍보 전략이 필요하다. 편집자 누구도 그 일을 할 줄 몰랐고, 그 일을 할 시간은 더더욱 없었다. 이들은 모두 전업 연구자다. 강의하고 실험하고 학생을 지도하면서, 계약상 의무가 아닌 그 모든 노동을 ‘공동체에 대한 기여’라는 이름으로 무상으로 떠안아야 했다. 학술 출판 산업이 저자와 심사자의 공짜 노동에 기생한다는 비판은 익숙하다. 그런데 다이아몬드 OA는 그 공짜 노동을 출판사로부터 학자에게로 옮겨놓을 뿐, 노동 자체를 없애지 못한다. 창간사의 표현대로, 이상은 풍요로운데 사람은 시간이 모자랐다.
둘째는 숨은 노동이다. 동료심사, 편집, 공동체 구축—학계를 떠받치는 이 보이지 않는 노동은 어떤 업무 분장표에도 잡히지 않는다. 더 개방적인 모델일수록 이 무급 노동에 더 깊이 의존한다는 역설을, 정작 그 역설을 논문으로 써온 사람들이 제 몸으로 겪었다.
셋째가 가장 아프다. 바로 변방의 현실이다. 소속 없는 다이아몬드 저널은 글로벌 사우스의 연구자들에게는 그림의 떡이다. 그들의 평가 시스템은 인정받는 출판사와의 제휴, 그리고 Scopus나 ISI 색인 등재를 요구하기 때문이다. 색인되지 않은 저널에 실린 논문은, 아무리 훌륭해도 그 나라에서는 실적으로 인정받지 못한다. 카자흐스탄의 한 연구자는 박사논문 인터뷰에서 이렇게 말했다. 박봉에 1200달러를 들여 스코퍼스에 논문을 실었고, 그것이 가족의 살림을 심각하게 압박했다고. 매년 한 편씩 의무적으로 내야 하는, 오직 그 요구를 채우기 위한 논문이라고. 로스-헬라우어가 일찍이 『네이처』에 썼던 한 문장이 떠오른다. 잘못 시행된 오픈 사이언스는 불평등을 심화시킨다는 것.
그래서 그들은 선택했다. 공증인 사무실에서 그들은 공동체를 대표할 협회를 세우려 했는데, 공증인은 이렇게 조언했다고 한다. 자신의 일은 법적 구조를 설계해 의뢰인의 이익을 보호하는 것인데, “민주화는 당신들의 이익에 대한 위협”이라고. 그러나 그들이 법적 형태로 새기고 싶었던 것은 자신들의 이익이 아니라 넓은 공동체의 이익이었다. 그렇게 ‘RORATION’이라는 협회가 태어났다. roration은 ‘새벽이슬(dewfall)’의 동의어다. 새 저널 여정의 새벽을 뜻하는, 의도된 작명이다.

RORATION은 저널을 소유하고 편집장을 임명한다. 저널의 이름과 지배구조와 지적재산권은 그 공동체가 누가 되든 그 공동체의 손에 남는다. 다이아몬드 OA의 핵심 가치인 ‘공동체 소유’를 이렇게 지켜낸 뒤, 그들은 정작 출판은 테일러 앤 프랜시스라는 거대 상업 출판사에 맡겼다. OA 운동가들에게는 변절로 보일 수 있는 선택이다. 자신들이 도망쳐 나온 바로 그 상업 출판의 품으로 되돌아간 것이니까. 그러나 그들은 이 선택을 변명하지 않는다. 그들은 가장 특권 없는 동료들의 필요에 더 큰 가중치를 두기로 했다고 적는다. 머리와 가슴 중 무엇을 따를 것인가의 문제에서, 그들은 이상의 순수함 대신 변방 동료들의 생존을 택했다.
이것이 ‘순수의 값’이다. 순수한 다이아몬드 OA는 그것을 감당할 시간과 인프라와 평판자본을 가진 글로벌 노스의 정착 연구자에게나 가능한 사치였다. 순수를 고집하는 순간, OA가 해방시키겠다던 바로 그 변방의 약자들이 가장 먼저 배제된다.
교리가 된 혁명
여기서 잠시, 내가 지난 칼럼들에서 했던 이야기로 돌아가야겠다. J·ROR의 고백은 진공에서 나온 것이 아니라, 오픈액세스 운동 사반세기의 변질이라는 더 큰 맥락 위에 놓여 있기 때문이다.
오픈액세스는 혁명으로 시작했다. 2000년대 초 부다페스트와 베를린에 모인 학자들은 물었다. 세금으로 만든 지식을 왜 돈 낸 사람만 읽어야 하는가. 지극히 옳은 분노였다. 누구나 공짜로 읽게 하자. 그러나 사반세기가 지난 지금, 바뀐 것은 착취의 구조가 아니라 청구서의 수신인뿐이다. 예전엔 ‘읽는 자’가 구독료를 냈다면, 이제는 ‘쓰는 자’가 게재료를 낸다. 『네이처』에 논문 한 편 싣는 값이 1700만 원, 신참 연구원 반년 치 월급이다. 전 세계가 게재료로 쓴 돈은 4년 사이 1조 2000억 원에서 3조 4000억 원으로 세 배 가까이 불었고, 그사이 엘스비어의 모회사는 구글도 애플도 넘어서는 38퍼센트의 영업이익률을 거뒀다. 인류의 지식을 다루는 일이 검색 광고를 파는 일보다 남는 장사가 된 것이다. 올해 2월, 세계 최대 연구기관인 중국과학원이 일류 OA 저널 30여 곳에 더는 게재료를 대주지 않겠다고 선언한 이유는 단 하나, ‘가성비’였다. 가장 권위 있다는 저널들조차, 이제 그 값이 과학의 목을 조른다는 사실을 더는 숨길 수 없게 된 것이다.
그런데 이 변질 위에 한 겹의 변질이 더 쌓였다. 오픈액세스가 하나의 도덕적 시험이 되어버린 것이다. J·ROR 창간사가 가장 날카롭게 짚는 대목이 바로 여기다. 새로운 OA 모델은 더 이상 연구자가 그 가치에 동의하느냐 마느냐를 선택하는 문제로 제시되지 않는다. 그것은 따르지 않으면 반과학적 러다이트가 되는, 강제된 순응의 문제로 제시된다. 창간사의 표현을 빌리면, 일탈을 폄하하는 사회화된 규범성이다. 단일하고 지배적인 모델을 밀어붙이는 일은, 어떤 이유로든 그 융통성 없는 모델에 적응할 수 없는 사례들—글로벌 사우스의 기관, 연구중심이 아닌 대학, 더 젊고 더 불안정한 인력—을 간과하고 고립시킬 위험을 안는다.
이 지점에서 나는 무릎을 쳤다. 이것은 내가 약탈적 학술지를 두고 했던 이야기와 정확히 같은 구조이기 때문이다. ‘약탈적’이라는 낙인은 거의 언제나 변방을 향한다. 1700만 원을 받는 『네이처』는 명문이고, 몇백 달러를 받는 나이지리아의 작은 저널은 약탈자다. 그 경계선은 학문의 질이 아니라 권력의 지도를 따라 그어진다. 마찬가지로, ‘다이아몬드 OA가 아니면 변절’이라는 교리는 그 교리를 감당할 수 있는 중심부의 잣대로 변방을 단죄한다. 약탈자 블랙리스트와 OA 순수주의는, 둘 다 가난하지만 정직한 변방을 진짜 사기꾼과 한 솥에 뭉뚱그려 단죄하는 같은 도덕주의의 두 얼굴이다.
약탈자라는 거울
J·ROR의 가장 뼈아픈 증거가 여기 있다. 그들이 MDPI를 떠난 것은 『퍼블리케이션스』가 약탈적이어서가 아니었다. 그 저널은 게재료를 받지 않았다. 그들이 떠난 것은 그 저널이 약탈적이라는 ‘목록’과 ‘낙인’에 가까이 있었기 때문이고, 편집위원들이 그 낙인 때문에 자기 저널을 실적으로 쓸 수 없었기 때문이다. 질이 아니라 평판의 지도가, 색인 등재 여부가, 나라별 평가 목록이 그들을 내몰았다.
이것이 핵심이다. 약탈자는 병을 만든 자가 아니라 병의 증상이다. 그리고 OA 순수주의 역시 병의 치료제가 아니라 같은 병의 또 다른 증상이다. 둘 다 같은 질병에서 자라난 곰팡이다. 그 질병의 이름은 논문이 화폐가 된 평가 시스템이다.
논문 편수와 피인용 수와 대학 순위로 연구자를 평가하는 한, 그것을 조작하는 일은 합리적 선택이 된다. 그래서 논문공장의 가짜 논문은 1.5년마다 두 배로 늘어나고—합법적 논문이 두 배가 되는 데는 15년이 걸린다—AI는 존재하지 않는 참조문헌을 그럴싸하게 지어내며, 강의실에 한 번도 나타나지 않은 외국인 교수가 6년간 496편의 논문을 어느 대학 이름으로 찍어내자 그 대학의 순위가 올랐다. 논문공장도, AI 환각도, 학술용병도, 약탈적 저널도, 그리고 1700만 원짜리 게재료도—모두 같은 뿌리에서 자란 가지들이다. 출판 아니면 소멸이라는 압박이 학계를 지배하는 한, 논문은 진리를 적는 그릇이 아니라 살아남기 위한 화폐가 된다. 화폐가 된 논문 위에서는, 다이아몬드든 골드든 그린이든, 어떤 OA 색깔도 구원이 되지 못한다. 청구서의 수신인만 바뀔 뿐이다.
그러므로 OA의 모델을 두고 벌이는 교리 전쟁은, 사실 잘못된 전선(戰線)이다. 우리가 정말 물어야 할 것은 ‘어떤 OA가 순수한가’가 아니라 ‘무엇이 이 모든 왜곡을 만들어내는가’이다.
그래서, 교리를 버린다는 것
J·ROR이 내놓은 답은 모델이 아니라 태도다. 선언문이 아니라 지도. 하나의 ‘존재 방식’을 영원히 고수하는 대신, 증거에 따라 끊임없이 자신을 고쳐 쓰겠다는 것. 그들은 연구에 관한 연구를 출판하는 저널이자, 동시에 자기 자신을 대상으로 연구에 관한 연구를 수행하는 저널이 되겠다고 선언한다. 동료심사 방식과 편집 워크플로를 저널 안에서 실험하고, 그 결과를 투명하게 공개하겠다고. 자신이 틀릴 수 있음을, 모든 것을 옳게 해내지는 못했음을 창간사 첫머리에서부터 인정하면서.
나는 이 태도가 옳다고 생각한다. 교리를 버린다는 것은 가치를 버린다는 뜻이 아니다. 그것은 가치를 단 하나의 모델에 못 박지 않고, 증거 앞에서 겸손하게 열어두는 일이다. 지식의 해방이라는 OA의 원래 분노는 여전히 정당하다. 다만 그 분노를 실현하는 방법이 단 하나뿐이라고 우길 때, 해방의 깃발은 또 하나의 배제의 칼이 된다.
그러나—여기서 나는 이 고백문에 박수만 보낼 수는 없다. 정직함을 위해 한 가지를 더 말해야 한다. 실용주의는 항복으로 미끄러지기 쉬운 비탈이다. 도망쳐 나온 상업 출판사의 품으로 되돌아가면서, 공동체 소유라는 법적 외피를 둘렀다고 해서 그 안의 권력관계가 사라지는 것은 아니다. 테일러 앤 프랜시스가 게재료를 낮게 유지하겠다고 약속했다지만, 오늘의 거대한 과점 체제 역시 한때는 그런 약속 위에서 자라났다. 공증인의 말처럼 민주화가 이익에 대한 위협이라면, 그 위협을 끝까지 감수할 수 있을 때에만 공동체 소유는 빈말을 면한다. 교리도 항복도 아닌 제3의 길은, ‘영원한 잠정성’이라는 불편한 자리를 끝까지 지킬 때에만 길이 된다. 증거가 바뀌면 모델도 바꾸겠다는 약속을, 그들이 정말 지키는지 우리는 지켜봐야 한다.
그리고 무엇보다, 이 모든 것은 평가 시스템과 출판 과점의 사슬을 끊지 않는 한 끝내 헛일이 될 것이다. 사이허브도, 즉시 공개 협약도, 다이아몬드 OA도, RORATION도—숫자를 숭배하는 시스템이 그대로인 한, 논문공장은 규제의 틈을 비집고 새 형태로 진화할 것이다. J·ROR의 고백이 값진 이유는 그들이 정답을 찾았기 때문이 아니라, 정답이 모델에 있지 않다는 것을 정직하게 보여주었기 때문이다.
나는 다시 내 초파리 앞으로 돌아가야 한다. 나 또한 생활형 과학자이기 때문이다. 그리고 또 몇 해에 걸쳐 벽돌 한 장을 빚을 것이다. 초파리로 노벨상을 받은 허먼 멀러가 핵실험이 유전자에 남길 상처를 알리기 위해 평생 광장에 섰던 것처럼, 보통의 과학자도 더는 무균실 안에만 숨어 있을 수 없다.
오픈액세스는 한때 우리의 가장 아름다운 분노였다. 그러나 분노가 교리가 되면, 그것은 자신이 해방시키려던 사람들을 가장 먼저 단죄한다. roration—새벽이슬. 이슬은 교리처럼 군림하지 않는다. 밤새 소리 없이 내려앉아 마른 잎을 적실 뿐이다. 메타과학자들이 자기 이름에 새겨 넣은 그 단어처럼, 어쩌면 우리에게 필요한 것은 더 순수한 깃발이 아니라, 더 정직한 새벽일지 모른다.
그 벽돌이 정직한 탑이 될지, 남의 금고를 채우는 돌멩이가 될지는 실험대가 아니라 우리가 광장에서 던지는 질문에 달려 있다. 그리고 이제 그 질문은, 어떤 오픈액세스가 가장 순수한가가 아니다. 우리는 왜, 아직도, 벽돌의 진위가 아니라 벽돌의 개수로 서로를 저울질하는가.
참고: G. Derrick, S. Horbach, B. Penders, T. Ross-Hellauer, 「Introducing the Journal of Research on Research (J·ROR)」, J·ROR 1(1), 2026 / T. Klebel & T. Ross-Hellauer, 「The APC-Barrier and Its Effect on Stratification in Open Access Publishing」, Quantitative Science Studies, 2023 / T. Ross-Hellauer, 「Open Science, Done Wrong, Will Compound Inequities」, Nature, 2022 / 김우재, 「과학이 죽어가고 있다」, 주간경향 플라이룸 78 / 「논문 1편에 1700만원」, 주간경향 플라이룸 79.